肠道菌群于癌症是帮凶?
新闻来源: 发布时间:[2024-03-12]
肠道菌群
肠道菌群,这些在人体肠道内寄居的微生物,一直以来都在默默影响着我们的健康。它们与我们的生理机能息息相关,甚至有人将其视为人体内的“另一个器官”。然而,它们的角色远比我们想象的要复杂。近年来,关于肠道菌群与癌症关系的研究不断深入,引起了人们的高度关注。这些微生物,到底是癌症的敌人还是帮凶?在深入探讨这个问题之前,让我们先回顾一下关于肠道菌群的基础知识。肠道菌群是一个由多种微生物组成的复杂生态系统,它们通过与肠道的相互作用,影响着我们的消化、免疫等多个系统。正是由于这种密切的关系,肠道菌群对癌症的发生、发展也产生了深远的影响。
但是,你们知道吗?不同种族及民族之间的癌症发病率及死亡率有较大差异。Nature Reviews Cancer上发表的一篇观点评论文章,讨论了在结构性种族主义下,社会、社区及个体在饮食、环境、生活习惯、政策等方面的差异导致的肠道菌群差异如何影响癌症的种族及民族差异[1]。
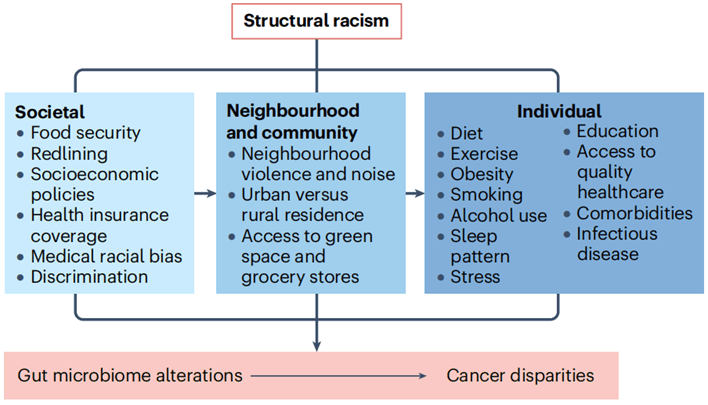
图1 影响肠道微生物群并进而导致癌症差异的多水平暴露
肠道微生物群与癌症之间是否具有因果关系,湘雅医院朱红利用公开数据库进行两个样本的孟德尔随机化(MR)计算[2],探究了并确认肠道微生物群与8种癌症类型存在一定的因果关系。比如,肠道微生物组遗传易感性与癌症之间存在11种因果关系,包括双歧杆菌属;肠道微生物组遗传易感性与癌症之间存在17种强烈的相关性,如双歧杆菌科和双歧杆菌目是乳腺癌症的危险因素,而瘤胃球菌属UCG013是预防乳腺癌症的保护因子等等。该研究有助于为微生物群介导的癌症的进一步机制和临床研究提供新的见解。
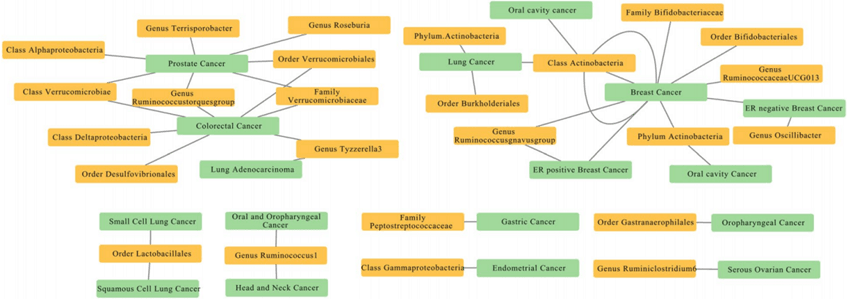
图2 孟德尔随机分析肠道菌群与癌症的因果关系
结直肠癌(CRC)的发病率呈上升趋势,已是全球癌症相关死亡的第二大原因,迫切需要改进预防和治疗策略。肠道内数万亿计的微生物构成了肠道微生物群,已被证实与CRC的发生和进展有密切关系。近日,Nature Reviews Microbiology发表综述文章[3],总结近期关于CRC患者肠道微生物群整体扰动和特定微生物与CRC之间关联的研究证据,阐述了微生物驱动CRC发生的潜在机制以及复杂微生物群落在CRC发病机制中的可能作用,并展望了针对微生物的CRC预防和治疗策略的临床应用前景。

图3 结直肠癌发病的微生物机制
在结直肠癌的研究中,肠道菌群与癌症之间的关系尤为引人关注。一些特定的肠道细菌被发现与结直肠癌的风险增加有关,而另一些细菌则可能具有保护作用。这些发现为未来癌症的预防和早期诊断提供了新的方向。在促成肠道菌群与癌症的因果关系中,肠道菌群产生的代谢物“功不可没”。它能够通过重塑肿瘤微环境并调节癌细胞和多种免疫细胞中的关键信号通路等机制,影响癌症的发生发展以及癌症治疗的效果。浙江省人民医院孟旭莉等团队在Advanced Science发表最新综述,详细阐述了肠道菌群代谢物影响癌症进展的机制以及在放疗、化疗和免疫治疗中的作用[4]。
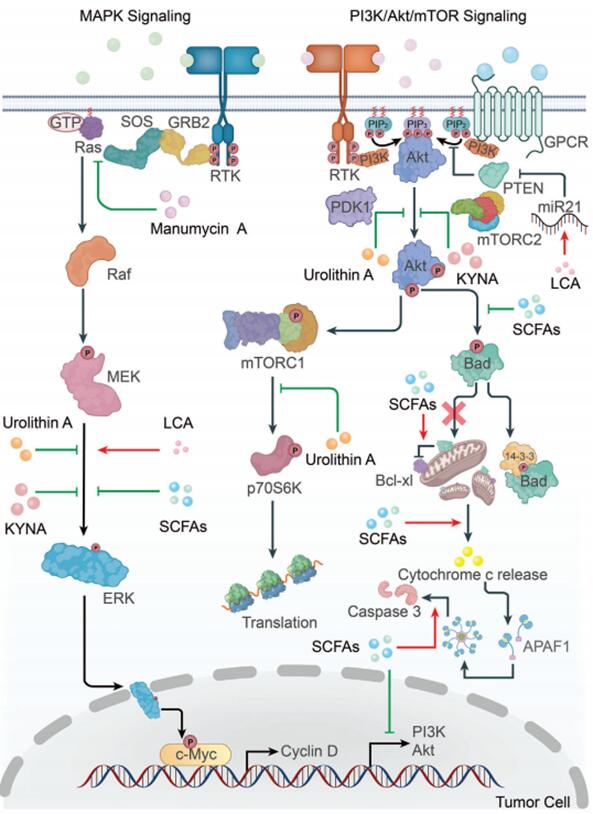
图4 微生物代谢物参与肿瘤细胞信号调节及肿瘤进展
微生物代谢物是连接肠菌和癌症的关键枢纽,通过重塑肿瘤微环境、影响免疫细胞功能和细胞因子水平来调节癌症进展;代谢物会调控MAPK、PI3K/Akt和Wnt等信号通路,影响肿瘤细胞增殖、凋亡和转移、减轻副作用提高放/化疗效果;除用抗生素破坏菌群的传统策略外,饮食、新药设计、粪菌移植、益生菌等基于微生物代谢物的新策略已被开发;治疗时,需综合考虑患者病情,避免代谢物与微生物、抗癌药间的冲突,导致药物无效或加剧其副作用。这将有助于更好地在癌症治疗中应用微生物代谢物并基于这些代谢物开发新的治疗策略,值得关注。
在治疗方面,微生物组也在癌症治疗中发挥了关键作用。例如,免疫检查点抑制剂的疗效受到肠道和肿瘤菌群的影响。此外,肠道细菌的代谢物在肿瘤进展和癌症治疗中也发挥重要作用。这些发现为未来的癌症治疗提供了新的思路和潜在的治疗靶点。
在过去的十年中,癌症治疗经历了从传统疗法向免疫检查点抑制剂(ICI)转变的革命。这些免疫疗法能够激发宿主免疫系统对抗肿瘤,并取得了前所未有的持久缓解效果。Trends in Molecular Medicine的综述文章探讨了细菌在重塑肿瘤免疫应答方面的出人意料的作用。利用共生菌群和肿瘤微生物组的研究有望发现哪些患者可以从免疫疗法中受益,并有助于扩大ICI治疗范围,提高治疗效果[5]。
研究发现,肠道菌群多样性高的癌症病人对免疫检查点抑制剂(ICI)疗法响应更好;肠道和肿瘤内微生物可直接下调免疫细胞的免疫检查点表达水平,也可通过产生吲哚、肌苷和短链脂肪酸等代谢物动员抗肿瘤免疫细胞;肠道菌群可减少肠炎等ICI相关副反应;菌群失衡可能导致炎症因子的过度产生,加重ICI疗法的副作用;临床上可运用膳食、益生元、益生菌、粪菌移植和抗生素等来改善肠道菌群组成和ICI疗效。
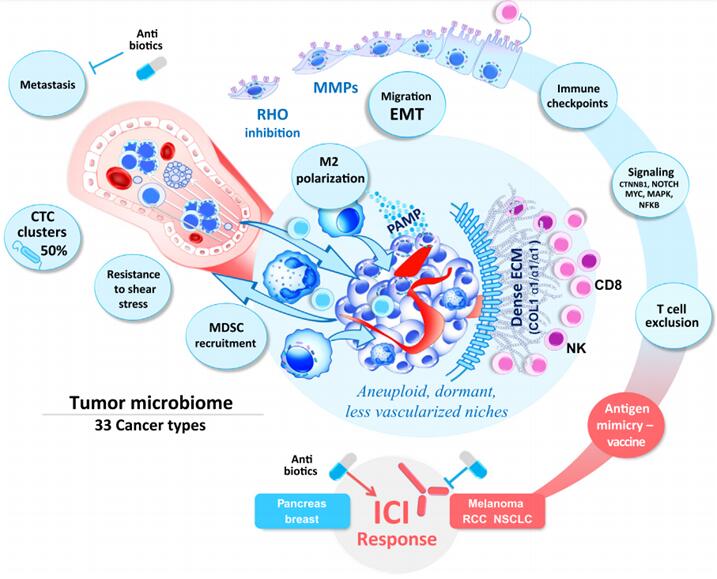
图5 肿瘤内细菌在肿瘤进展中的驱动作用
癌症与肠道菌群之间的关系是一个复杂而多维的话题,越来越多的证据表明,微生物组在癌症的发展和治疗中扮演着重要角色,但菌群对于癌症是敌还是帮凶,应具体问题具体分析。
总体而言,肠道菌群在癌症的发展和治疗中发挥着不容忽视的作用。虽然我们仍需进一步探索其具体机制和潜在的治疗策略,但这些研究结果无疑为未来的癌症研究开辟了新的方向。在未来的研究中,我们需要更深入地了解肠道菌群与癌症之间的相互作用,以便为患者提供更有效的个性化治疗方案。
参考文献
[1]Byrd D, Wolf P. The microbiome as a determinant of racial and ethnic cancer disparities. Nat Rev Cancer. 2023 Oct 23.
[2]Long Y, Tang L, Zhou Y, Zhao S, Zhu H. Causal relationship between gut microbiota and cancers: a two-sample Mendelian randomisation study. BMC Med. 2023 Feb 21;21(1):66.
[3]White MT, Sears CL. The microbial landscape of colorectal cancer. Nat Rev Microbiol. 2023 Oct 4.
[4]Yang Q, Wang B, Zheng Q, Li H, Meng X, Zhou F, Zhang L. A Review of Gut Microbiota-Derived Metabolites in Tumor Progression and Cancer Therapy. Adv Sci (Weinh). 2023 May;10(15):e2207366.
[5]Guillot N, Roméo B, Manesh SS, Milano G, Brest P, Zitvogel L, Hofman P, Mograbi B. Manipulating the gut and tumor microbiota for immune checkpoint inhibitor therapy: from dream to reality. Trends Mol Med. 2023 Nov;29(11):897-911.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!